Merido News – 11/2023
 17 marca 2023
17 marca 2023 O czym należy pamiętać przy serializacji leków w systemie PLMVS / KOWAL?
O czym należy pamiętać przy serializacji leków w systemie PLMVS / KOWAL?
Weryfikacja autentyczności leków jest z nami na dobre. Przygotowaliśmy krótki przegląd kilku najczęściej pojawiających się tematów na jakie napotykamy podczas kontaktu z Państwem.
– Anulowanie wycofania leku z systemu KOWAL/ NMVS możliwe jest do 10 dni od momentu wycofania, po upływie 10 dni przywrócenie opakowania na stan nie będzie możliwe.
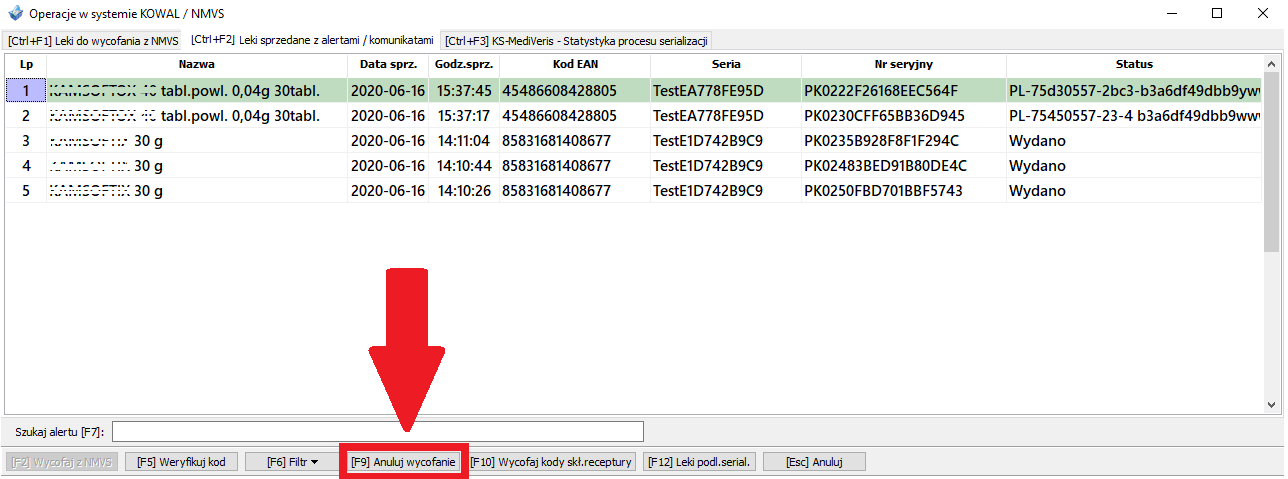
– Zwracając lek do hurtowni, należy pamiętać o zmianie statusu leku na AKTYWNY, w innym przypadku hurtownia może odrzucić zwrot. Opisany powyżej limit czasowy 10 dni płynie od momentu wycofania danego leku, dlatego sugerujmy, aby nie zwlekać z przywróceniem statusu produktu w Systemie PLMVS. Hurtownia, która otrzymała z apteki zwrot leku, ma obowiązek zweryfikowania tego produktu w PLMVS.
– Po pojawieniu się Alertu w pierwszej kolejności należy sprawdzić poprawność danych na opakowaniu, tzn. czy dane odczytane z kodu 2D w oprogramowaniu są w pełni zgodne z tymi nadrukowanymi na opakowaniu danego leku. W przypadku nieczytelnego kodu 2D Data Matrix istnieje możliwość ręcznego wprowadzenia danych w celu weryfikacji opakowania produktu serializowanego. Zgodnie z zaleceniami Komisji Europejskiej, jeżeli możliwa jest weryfikacja danych produktu na podstawie danych czytelnych dla ludzi, produkt można dystrybuować. W przypadku, kiedy zarówno dane czytelne dla ludzi oraz kod 2D nie są czytelne, nie zaleca się dalszej dystrybucji produktu.
– Przy przenoszeniu do kolejki pozycji podlegającej serializacji:
Realizujemy sprzedaż dla pacjenta wybierając z listy towar podlegający serializacji, program poprosi użytkownika o zeskanowanie kodu 2D.
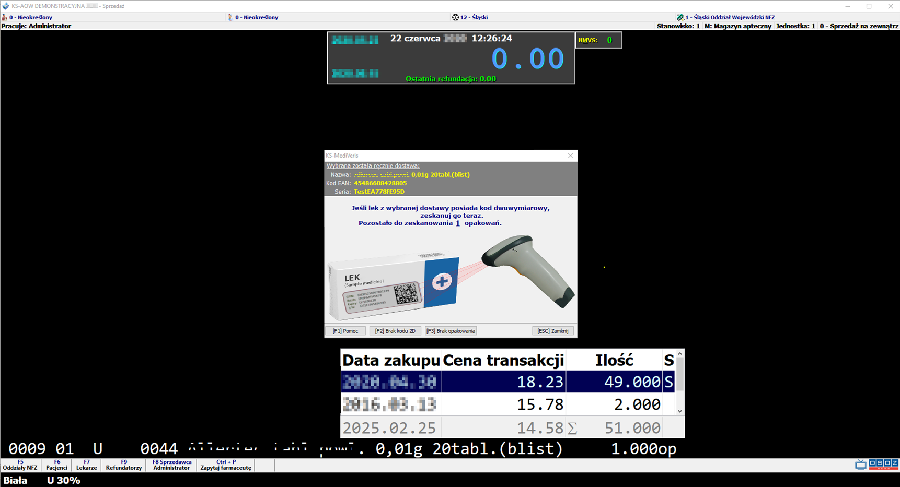
Po zeskanowaniu kodu 2D i zatwierdzeniu sprzedaży za pomocą funkcji ALT+F10 przenosimy pozycje do kolejki.
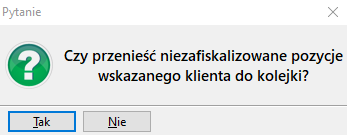
Następnie zatwierdzamy komunikat i pobieramy zaliczkę. Dodatkowo na ekranie wyświetli się informacja, że do kolejki dodawane są opakowania leków podlegające serializacji. Podczas wydania tych opakowań pacjentowi konieczne będzie wycofanie unikalnych identyfikatorów opakowań z systemu NMVS. Użytkownik powinien na tym etapie zdecydować czy zatwierdzić komunikat przyciskiem TAK (pacjent dostaje opakowania) czy też wybrać odpowiedź NIE (pacjent po odbiór opakowania przyjdzie w innym terminie).

Jeżeli użytkownik zdecydował, że system ma wycofać opakowania leków z NMVS (na pytanie odpowiedział TAK), podczas sprzedaży z kolejki system nie poprosi o ponowne zeskanowanie kodu. Natomiast w przypadku, gdy użytkownik zdecydował, że program ma NIE wycofywać opakowań z systemu NMVS, to w momencie wydania pozycji podlegających serializacji z kolejki program poprosi o zeskanowanie kodu dwuwymiarowego z wydawanego pacjentowi opakowania.
 Jakie zmiany w programie KS-Apteka pojawiły się w ostatnich dniach?
Jakie zmiany w programie KS-Apteka pojawiły się w ostatnich dniach?
.
Zmiany w module APW11 z dnia 2023.03.17 [2023.1.3.0]
- Dodano blokadę sprzedaży leku z uprawnieniem Senior w ramach realizacji e-Recepty wystawionej przez felczera. Program pozwoli wydać lek z pominięciem tego uprawnienia.
- Wniosek: Dodano nowe uprawnienia (na liście uprawnień do wyboru) dla osób, o których mowa w art. 37b ust. 1 ustawy o pomocy obywatelom Ukrainy, w związku z konfliktem zbrojnym na terytorium tego państwa w zakresie wynikającym z art. 37 ust. 1 tej ustawy oraz dla osób, o których mowa w art. 2 ust. 1 pkt 3 lit. c ustawy o świadczeniach.
Zmiany w module APW21 z dnia 2023.03.17 [2023.1.3.0]
- Eksport do SAP (wzór 3). Poprawiono przekazywanie kwot dla form płatności w przypadku płatności mieszanej.
- Środki pomocnicze: w raportowaniu z NFZ: dodano obsługę nowych uprawnień dla osób, o których mowa w art. 37b ust. 1 ustawy o pomocy obywatelom Ukrainy, w związku z konfliktem zbrojnym na terytorium tego państwa w zakresie wynikającym z art. 37 ust. 1 tej ustawy oraz dla osób, o których mowa w art. 2 ust. 1 pkt 3 lit. c ustawy o świadczeniach.
Zmiany w module APW23 z dnia 2023.03.17 [2023.1.3.0]
- Rozbudowano zestawienie „Sprzedaż leków zawierających substancje
psychoaktywne”:
* do przeglądu i wydruku dodano kolumnę z numerem jednostki organizacyjnej dla aptek z licencją na wielomagazynowość,
* dodano filtr ograniczający przegląd i wydruk do pozycji z przekroczeniami.
 Czy widzieliście obwieszczenie dotyczące nowej listy leków zagrożonych brakiem dostępności w marcu 2023?
Czy widzieliście obwieszczenie dotyczące nowej listy leków zagrożonych brakiem dostępności w marcu 2023?
.
W Dzienniku Urzędowym Ministra Zdrowia opublikowano nową listę produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych zagrożonych brakiem dostępności na terytorium Rzeczypospolitej Polskiej. Na nowej liście jest aż 256 leków. Wśród nowych pozycji, które umieszczono w wykazie znajdują się między innymi insuliny takie jak: Gensulin M30 (30/70), Gensulin M40 (40/60), Gensulin M50 (50/50), Gensulin N, Gensulin R; Humalog, Humalog Mix 25, Humalog Mix 50; Humulin M3 (30/70), Humulin N, Humulin R; Insulin aspart Sanofi, Insulin lispro Sanofi; Insuman Basal, Insuman Comb 25, Insuman Rapid.
Informujemy, że Baza KS-BLOZ od dnia 14 marca 2023 r. zawiera produkty oznaczone znacznikiem „Odmowa realizacji” zgodne z: „Obwieszczeniem Ministra Zdrowia z dnia 13 marca 2023 r. w sprawie wykazu produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych zagrożonych brakiem dostępności na terytorium Rzeczypospolitej Polskiej na dzień 15 marca 2023 r.”. (D. Urz. M. Z. z dnia 13.03.2023, poz. 21).
W systemie aptecznym KS-AOW podczas aktualizacji bazy KS-BLOZ z poziomu modułu APW44 Komunikacja – CTRL+1 Pełny KS-BLOZ dodatkowy znacznik „Wymagane wysyłanie odmów realizacji do GIF” przenosi się automatycznie na apteczną kartę towaru.
 Jakie leki pojawiły się w najnowszym wykazie braków GIF?
Jakie leki pojawiły się w najnowszym wykazie braków GIF?
.
Jak co dwa tygodnie Główny Inspektor Farmaceutyczny przygotował zestawienie produktów leczniczych o utrudnionej dostępności na terytorium Polski. Z informacji podanych przez GIF wynika, że na rynek wróciły produkty lecznicze takie jak:
- Hepa-Merz 3000, Ornithini aspartas, Granulat do sporządzania roztworu doustnego 3 g/5 g, 30 sasz. 5 g;
- Euthyrox N 50 Levothyroxinum natricum, tabletki, 50 mcg, 50 tabl.;
- Tulip, Atorvastatinum, tabletki powlekane, 20 mg, 30 tabl.;
- Euthyrox N 50, Levothyroxinum natricum, tabletki, 50 mcg, 100 tabl.;
- ALDARA, Imiquimodum krem, 5 mg/100 mg (5%), 12 saszetek;
- Duracef, Cefadroxilum kapsułki, 500 mg, 20 kaps.;
- Lamilept, Lamotriginum, tabletki, 100 mg x 30 szt., 30 tabl.;
- Locoid Crelo, Hydrocortisoni butyras, emulsja, 1 mg/g, 1 butelka 30 g;
- Duracef, Cefadroxilum kapsułki, 500 mg, 20 kaps.;
- Duracef, Cefadroxilum, kapsułki, 500 mg, 12 kaps.;
- AMOKSIKLAV Amoxicillinum + Acidum clavulanicum, tabletki powlekane, 875 mg + 125 mg 14 tabl.;
- Ceclor MR, Cefaclorum tabletki powlekane o przedłużonym uwalnianiu375 mg x 10 szt. 10 tabl.;
- Ospen 1500, Phenoxymethylpenicillinum kalicum, Tabletki powlekane 1 500 000 j.m. 12 tabl.
- Tegretol CR 200, Carbamazepinum, Tabletki o zmodyfikowanym uwalnianiu 200 mg 50 tabl.